Scopus, KCI, KoreaMed

Articles
- Page Path
- HOME > J Clin Nutr > Volume 12(1); 2020 > Article
- Original Article Incidence of Potential Intravenous Drug Incompatibilities in the Intensive Care Units of a University Hospital
-
Sunmin Lee

- 일개 대학병원 성인 중환자실에서 투약된 주사제의 비호환성 발생률 조사
-
이선민

-
Journal of Clinical Nutrition 2020;12(1):14-20.
DOI: https://doi.org/10.15747/jcn.2020.12.1.14
Published online: June 30, 2020
Department of Pharmacy, Inha University Hospital, Incheon, Korea
- Correspondence to Sunmin Lee https://orcid.org/0000-0002-0528-5098Department of Pharmacy, Inha University Hospital, 27 Inhang-ro, Jung-gu, Incheon 22332, KoreaTel: +82-32-890-3311, E-mail: monoamin@naver.com
© 2020, The Korean Society for Parenteral and Enteral Nutrition. All Rights Reserved.
This is an open-access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
- 1,761 Views
- 24 Download
- 1 Crossref
Abstract
-
Purpose Potential incompatibility (PI) between drugs infused together is frequent but under-recognized in intensive care units (ICU). This paper describes the frequency of the inappropriate coadministration of infused medications via the Y-site and identifies the most frequent and relevant drug incompatibilities in a single-center, cross-sectional observational study.
-
Methods This research was a retrospective cross-sectional study of 100 patients conducted between July and December 2019 in an ICU. The medical records of 100 patients in the ICU were collected, and their compatibility was assessed based on published compatibility data.
-
Results PI was detected in approximately 48.5% of patients (1.5 incompatibility/patient ratio). Most incompatibilities detected were classified as follows: the untested (84.4%), variable (9.7%), incompatibility (3.9%), or no data (1.9%). Acetylcysteine was the most frequent drug implied in PI. A difference was observed between the lengths of ICU and PI incidences (P=0.01). In the correlation between PI and APACHE II (Acute Physiology and Chronic Health Evaluation II), there was a weak correlation between APACHE II and PI (r=0.283, P<0.05).
-
Conclusion PI is common in an ICU, with a higher prevalence of non-tested incompatibilities. The number of drugs and prescription of acetylcysteine, pantoprazole, meropenem piperacillin/tazobactam, or phytonadione are the risk factors for PI.
서 론
대상 및 방법
결 과
고 찰
| Medication use (n=630) | Value |
|---|---|
| Prevalence of inappropriate combinations administered via Y-site connector | |
| Incompatible pairs | 154 |
| Patient with PI | 48 (48.5) |
| Reasons for inappropriate combinations | |
| Incompatibility | 6 (3.9) |
| Variablea | 15 (9.7) |
| Untestedb | 130 (84.4) |
| No datac | 3 (1.9) |
| Potential incompatibility/patient ratio | 1.5 |
| Potential incompatibility | Drug pairs | n (%) |
|---|---|---|
| Most frequent incompatible pairs | Pantoprazole- Meropenem | 2 (33.3) |
| Most frequent incompatible drug | Pantoprazole | 4 (33.3) |
| Most frequent variablea pairs | Pantoprazole-Piperacillin tazobactam | 5 (33.3) |
| Most frequent variablea drug | Pantoprazole | 9 (30.0) |
| Most frequent untestedb pairs | Acetylcysteine- Phytonadione | 15 (11.5) |
| Most frequent untestedb drug | Acetylcysteine | 83 (31.9) |
| Demographic and clinical characteristic | PI | ||
|---|---|---|---|
|
|
|||
| Mean | Standard deviation | P-value | |
| Sex | 0.05 | ||
| Male | 1.9 | 2.8 | |
| Female | 1.0 | 1.6 | |
| ICU stays (d) | 0.01* | ||
| 1∼6 | 1.1 | 2.1 | |
| ≥7 | 2.8 | 3.0 | |
| CVC | 0.2 | ||
| With CVC | 2.0 | 2.2 | |
| Without CVC | 1.3 | 2.5 | |
| APACHE II (n=72) | r=0.283* | ||
- 1. Secoli SR, Pérez-Esquirol E, de Las Heras-Matellán MJ, Vendrell-Bosh L, Ballarín-Alins E. [Incompatibilities in intravenous therapy: what can be done to prevent them?]. Enferm Clin 2009;19(6):349-53; Spanish. PubMed
- 2. Newton DW. 2009;Drug incompatibility chemistry. Am J Health Syst Pharm 66(4):348-57. ArticlePubMed
- 3. Machotka O, Manak J, Kubena A, Vlcek J. 2015;Incidence of intravenous drug incompatibilities in intensive care units. Biomed Pap Med Fac Univ Palacky Olomouc Czech Repub 159(4):652-6. ArticlePubMed
- 4. Taxis K, Barber N. 2004;Incidence and severity of intravenous drug errors in a German hospital. Eur J Clin Pharmacol 59(11):815-7. ArticlePubMedPDF
- 5. McNearney T, Bajaj C, Boyars M, Cottingham J, Haque A. 2003;Total parenteral nutrition associated crystalline precipitates resulting in pulmonary artery occlusions and alveolar granulomas. Dig Dis Sci 48(7):1352-4. ArticlePubMedPDF
- 6. Boehne M, Jack T, Köditz H, Seidemann K, Schmidt F, Abura M, et al. 2013;In-line filtration minimizes organ dysfunction: new aspects from a prospective, randomized, controlled trial. BMC Pediatr 13:21.ArticlePubMedPMCPDF
- 7. McKinnon BT. FDA safety alert: hazards of precipitation associated with parenteral nutrition. Nutr Clin Pract 1996;11(2):59-65. ArticlePubMed
- 8. Steadman E, Raisch DW, Bennett CL, Esterly JS, Becker T, Postelnick M, et al. 2010;Evaluation of a potential clinical interaction between ceftriaxone and calcium. Antimicrob Agents Chemother 54(4):1534-40. ArticlePubMedPMCPDF
- 9. Bradley JS, Wassel RT, Lee L, Nambiar S. 2009;Intravenous ceftriaxone and calcium in the neonate: assessing the risk for cardiopulmonary adverse events. Pediatrics 123(4):e609-13. ArticlePubMedPDF
- 10. Kanji S, Lam J, Goddard RD, Johanson C, Singh A, Petrin L, et al. 2013;Inappropriate medication administration practices in Canadian adult ICUs: a multicenter, cross-sectional observational study. Ann Pharmacother 47(5):637-43. ArticlePubMedPDF
- 11. Kanji S, Lam J, Johanson C, Singh A, Goddard R, Fairbairn J, et al. 2010;Systematic review of physical and chemical compatibility of commonly used medications administered by continuous infusion in intensive care units. Crit Care Med 38(9):1890-8. ArticlePubMed
- 12. Lee S. 2020;Development of a two-dimensional compatibility table for intravenous Y-site drug administration in a Neonatal Intensive Care Unit. J Korean Soc Health-syst Pharm 37(1):64-73. Article
- 13. Camut A, Noirez V, Gustin B, Khalife A. 2007;Improvement of antibiotics infusion practices: proposition and evaluation of a good practices' guide. J Pharm Clin 26(3):143-50.
- 14. Vogel Kahmann I, Bürki R, Denzler U, Höfler A, Schmid B, Splisgardt H. 2003;[Incompatibility reactions in the intensive care unit. Five years after the implementation of a simple "colour code system"]. Anaesthesist 52(5):409-12; German. PubMed
- 15. Maison O, Tardy C, Cabelguenne D, Parat S, Ducastelle S, Piriou V, et al. 2019;Drug incompatibilities in intravenous therapy: evaluation and proposition of preventive tools in intensive care and hematology units. Eur J Clin Pharmacol 75(2):179-87. ArticlePubMedPDF
- 16. Marsilio NR, da Silva D, Bueno D. 2016;Drug incompatibilities in the adult intensive care unit of a university hospital. Rev Bras Ter Intensiva 28(2):147-53. ArticlePubMedPMC
- 17. Castells Lao G, Rodríguez Reyes M, Roura Turet J, Prat Dot M, Soy Muner D, López Cabezas C. 2020;Compatibility of drugs administered as Y-site infusion in intensive care units: a systematic review. Med Intensiva 44:80-7. ArticlePubMed
- 18. Bertsche T, Mayer Y, Stahl R, Hoppe-Tichy T, Encke J, Haefeli WE. Prevention of intravenous drug incompatibilities in an intensive care unit. Am J Health Syst Pharm 2008;65(19):1834-40. ArticlePubMed
- 19. Colldén H, Teimori K, Asadian R. 2015;[Compatibility of intravenous medications needs attention. Catheter occlusion, treatment failure and embolisms can be prevented]. Lakartidningen 112:DMP6; Swedish. PubMed
- 20. Taniguchi T, Yamamoto K, Kobayashi T. 1998;Precipitate formed by thiopentone and vecuronium causes pulmonary embolism. Can J Anaesth 45(4):347-51. ArticlePubMedPDF
- 21. Longuet P, Lecapitaine AL, Cassard B, Batista R, Gauzit R, Lesprit P, et al. 2016;Preparing and administering injectable antibiotics: how to avoid playing God. Med Mal Infect 46(5):242-68. ArticlePubMed
References
Figure & Data
REFERENCES
Citations

- Impact of Implementing a Computerized Injectable Drug-Solution Compatibility Program
Sang-Hee Hong, Na-Young Kim, Seo-Hyun Ahn, Hye-Lim Ahn, Mi-Na Min, Jin-Suk Kang
Journal of Korean Society of Health-System Pharmacists.2025; 42(2): 140. CrossRef
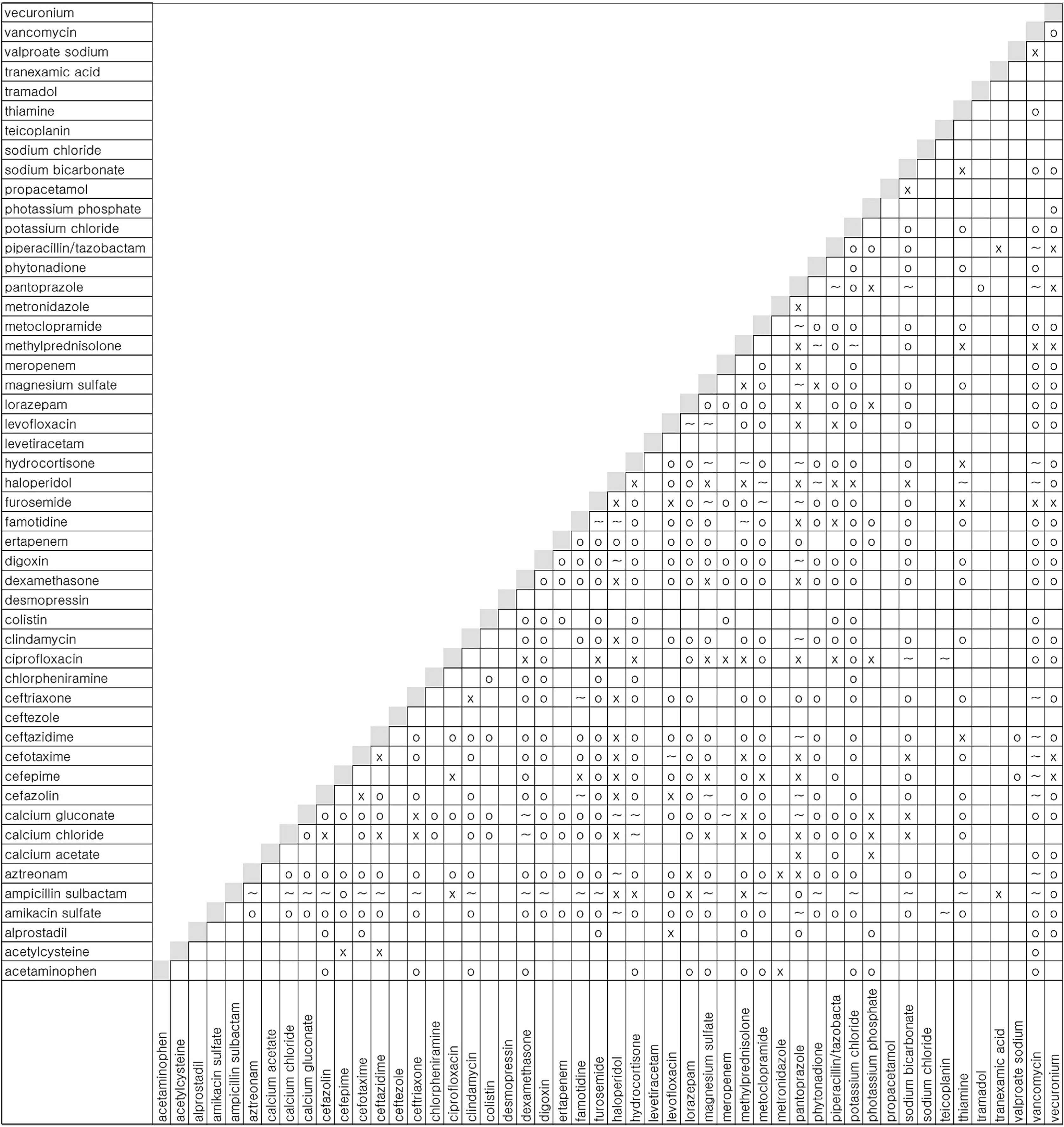
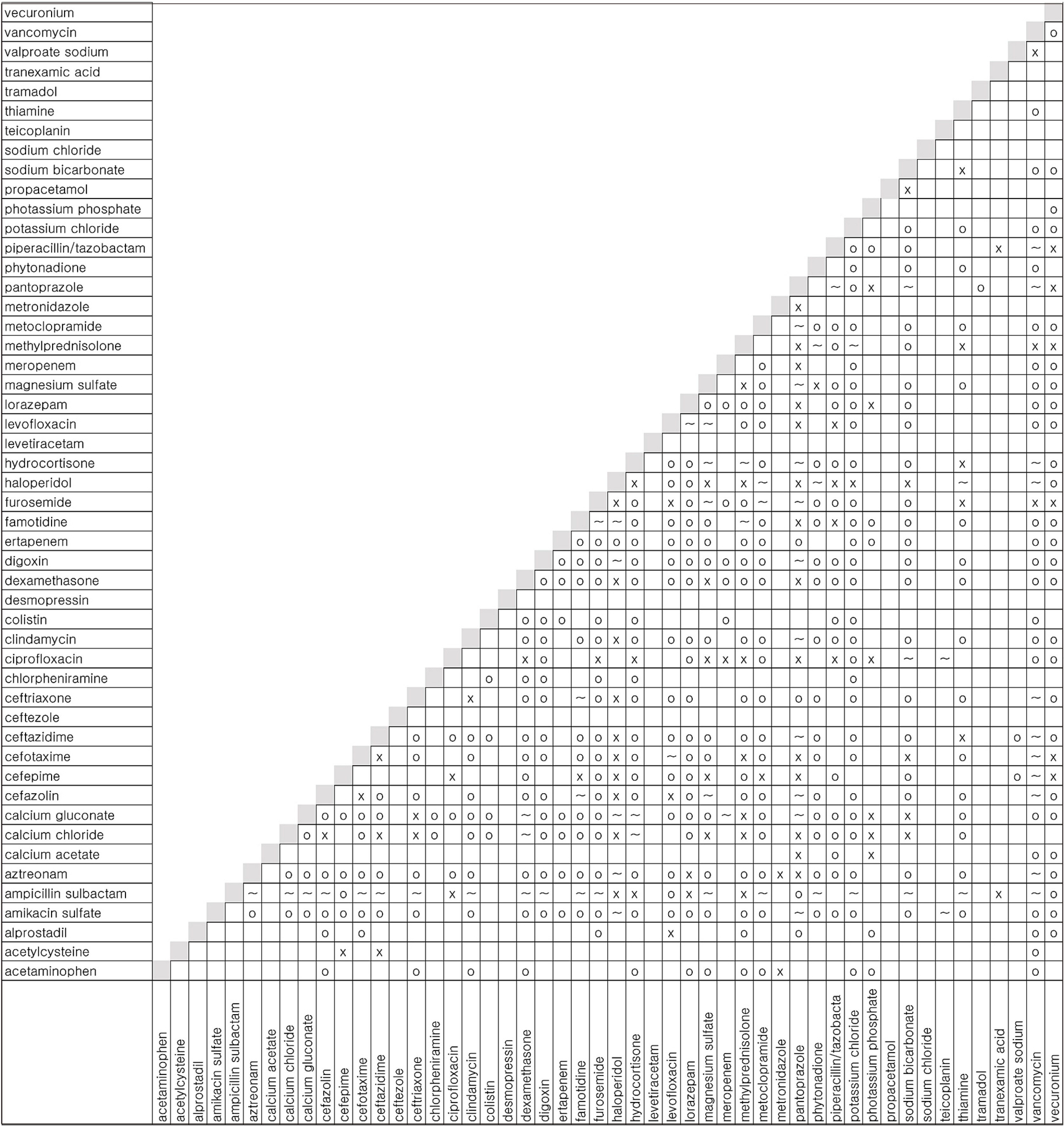
Fig. 1
Sample characteristics
| Demographic and clinical characteristic | Patient (n=99) |
|---|---|
| Sex male | 61 (61.6) |
| Age (y) | 64.8±18.5 (13∼98) |
| Intensive care unit stay (d) | 5.8±6.0 (2∼42) |
| Number of intravenous medications | 6.3±4.0 |
| APACHE II (n=72) | 15.3±9.7 |
| CVCs inserted patient | 33 (33.3) |
| Primary reason for intensive care unit admission | |
| Sepsis | 8 (8.1) |
| Drug intoxication | 6 (6.1) |
| Cerebral infarction | 6 (6.1) |
| CAOD | 4 (4.0) |
| ICH | 4 (4.0) |
| Septic shock | 4 (4.0) |
| Others | 67 (67.7) |
Values are presented as number (%) or mean±standard deviation (range).
APACHE II = Acute Physiology and Chronic Health Evaluation II; CVC = central venous catheter; CAOD = coronary artery occlusive disease; ICH = intra-cerebral hemorrhage.
Prevalence of inappropriate combinations of coadministered medication infusions
| Medication use (n=630) | Value |
|---|---|
| Prevalence of inappropriate combinations administered via Y-site connector | |
| Incompatible pairs | 154 |
| Patient with PI | 48 (48.5) |
| Reasons for inappropriate combinations | |
| Incompatibility | 6 (3.9) |
| Variable |
15 (9.7) |
| Untested |
130 (84.4) |
| No data |
3 (1.9) |
| Potential incompatibility/patient ratio | 1.5 |
Values are presented as number only or number (%).
PI = potential incompatibility.
aConflicting Y-site data with compatible and incompatible results. bNo Y-site stability data available for ≥2 combinations. cNo data on Micromedex.
The most frequent drug and drug pairs involved in potential incompatibility
| Potential incompatibility | Drug pairs | n (%) |
|---|---|---|
| Most frequent incompatible pairs | Pantoprazole- Meropenem | 2 (33.3) |
| Most frequent incompatible drug | Pantoprazole | 4 (33.3) |
| Most frequent variable |
Pantoprazole-Piperacillin tazobactam | 5 (33.3) |
| Most frequent variable |
Pantoprazole | 9 (30.0) |
| Most frequent untested |
Acetylcysteine- Phytonadione | 15 (11.5) |
| Most frequent untested |
Acetylcysteine | 83 (31.9) |
aConflicting Y-site data. bNo Y-site stability data available for ≥2 combinations.
Risk factors for potential intravenous drug incompatibility
| Demographic and clinical characteristic | PI | ||
|---|---|---|---|
| Mean | Standard deviation | P-value | |
| Sex | 0.05 | ||
| Male | 1.9 | 2.8 | |
| Female | 1.0 | 1.6 | |
| ICU stays (d) | 0.01 |
||
| 1∼6 | 1.1 | 2.1 | |
| ≥7 | 2.8 | 3.0 | |
| CVC | 0.2 | ||
| With CVC | 2.0 | 2.2 | |
| Without CVC | 1.3 | 2.5 | |
| APACHE II (n=72) | r=0.283 |
||
PI = potential incompatibility; ICU = intensive care unit; CVC = central venous catheter; APACHE II = Acute Physiology and Chronic Health Evaluation II.
*P<0.05.
Values are presented as number (%) or mean±standard deviation (range). APACHE II = Acute Physiology and Chronic Health Evaluation II; CVC = central venous catheter; CAOD = coronary artery occlusive disease; ICH = intra-cerebral hemorrhage.
Values are presented as number only or number (%). PI = potential incompatibility. aConflicting Y-site data with compatible and incompatible results. bNo Y-site stability data available for ≥2 combinations. cNo data on Micromedex.
aConflicting Y-site data. bNo Y-site stability data available for ≥2 combinations.
PI = potential incompatibility; ICU = intensive care unit; CVC = central venous catheter; APACHE II = Acute Physiology and Chronic Health Evaluation II. *P<0.05.

 E-submission
E-submission KSPEN
KSPEN KSSMN
KSSMN ASSMN
ASSMN JSSMN
JSSMN Cite
Cite