Scopus, KCI, KoreaMed

Articles
- Page Path
- HOME > Surgical Metabolism and Nutrition > Volume 9(2); 2018 > Article
- ORIGINAL ARTICLE Recovery Pattern of the Nutritional Status after Surgical Treatment for Pancreatic Head Disease: Compared with Malignancy and Non-malignancy
- Eunjung Kim, M.S.1, Youngmin Han, M.S.2, Hongbeom Kim, M.D.2, Wooil Kwon, M.D., Ph.D.2, Sun-Whe Kim, M.D., Ph.D., FACS.2, Jin-Young Jang, M.D., Ph.D., FACS.2
- 췌장 두부 질환에 대한 수술적 치료 후 영양상태 회복 패턴: 악성 및 비악성 질환 비교
- 김은정, M.S.1, 한영민, M.S.2, 김홍범, M.D.2, 권우일, M.D., Ph.D.2, 김선회, M.D., Ph.D., FACS.2, 장진영, M.D., Ph.D., FACS.2
-
Surgical Metabolism and Nutrition 2018;9(2):51-58.
DOI: https://doi.org/10.18858/smn.2018.9.2.51
Published online: December 30, 2018
Department of Nutritional Support Team, Seoul National University Hospital, Seoul, Korea
Department of Surgery and Cancer Research Institute, Seoul National University College of Medicine, Seoul, Korea
- Correspondence to: Jin-Young Jang, Division of Hepatobiliary and Pancreatic Surgery, Department of Surgery, Seoul National University Hospital, Seoul National University College of Medicine, 101 Daehak-ro, Jongno-gu, Seoul 03080, Korea Tel: +82-2-2072-2194, Fax: +82-2-741-2194, E-mail: jangjy4@snu.ac.kr
Copyright: © The Korean Society of Surgical Metabolism and Nutrition
This is an open access article distributed under the terms of the Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
- 1,414 Views
- 3 Download
- 1 Crossref
Abstract
-
Purpose: Malnutrition affects the clinical outcomes of pancreatic disease. On the other hand, the changes in the nutritional status stratified by malignant and non-malignant diseases after surgery still need to be determined. The aim was to confirm the changing nutritional status and clinical outcomes after a pancreatoduodenectomy according to malignant and non-malignant disease.
-
Materials and Methods: Data were collected prospectively from 157 patients between 2009 and 2015. The nutritional status was classified as well-nourished, at-risk of malnutrition, and malnourished by a Mini Nutrition Assessment. The clinical outcomes were assessed using the postoperative complication, hospital stay, biochemical nutritional markers, and quality-of-life (QOL).
-
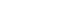
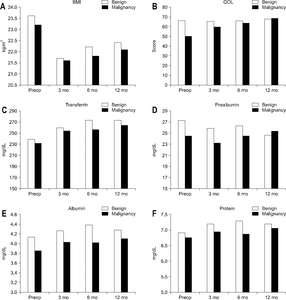
Results: Preoperatively, the proportion of malnourished status in the malignant disease group (group B) were 66.7% and 33.3% in the non-malignancy group (group A). The malnutrition rate in group B was higher than that in group A at 3, 6, and 12 months after surgery (58.1% vs. 41.9%, 90.0% vs. 10.0, 77.8% vs. 22.2%, respectively). The preoperative QOL was significantly lower in group B than in group A (P<.001); however, the QOL was comparable between the two groups after surgery. The body mass index was unrecovered after surgery in all groups.
-
Conclusion: Patients with malignant pancreatic disease are more likely to suffer from a poor nutritional status than those with non-malignant pancreatic disease. One year after the pancreatoduodenctomy, the at-risk of malnutrition and malnourished rate were found to be over 70% in all patients. Therefore, more efforts will be needed to improve the nutritional status in pancreatic head disease.
서 론
대상 및 방법
결 과
| Variables | Overall n=157 | Well-nourished n=32 (20.4%) | At risk n=101 (64.3%) | Malnourished n=24 (15.3%) | P-valve |
|---|---|---|---|---|---|
| Age (years) | 60.4±11.9 | 58.3±13.1 | 60.5±10.6 | 62.5±15.5 | 0.433 |
| Sex | 0.183 | ||||
| Male/Female | 80/74 | 14/6 | 47/45 | 19/23 | |
| Comorbidity: One or more | 94 (59.9%) | 16 (17.0%) | 63 (67.0%) | 15 (16.0%) | 0.442 |
| Previous Diabetes mellitus | 44928.0%) | 5 (15.6%) | 32 (31.7%) | 7 (29.2%) | 0.210 |
| Operation | 0.783 | ||||
| PD* | 24 (15.3%) | 6 (18.8%) | 14 (13.9%) | 4 (16.7%) | |
| PPPD† | 133 (84.7%) | 26 (81.3%) | 87 (86.1%) | 20 (83.3%) | |
| Diagnosis | 0.050 | ||||
| Benign | 77 (49.0%) | 21 (65.6%) | 48 (47.5%) | 8 (33.3%) | |
| Malignancy | 80 (51.0%) | 11 (34.4%) | 53 (52.5%) | 16 (66.7%) | |
| Stage I | 8 (10.0%) | 4 (36.4%) | 3 (5.7%) | 1 (6.5%) | |
| Stage II | 69 (86.3%) | 7 (63.6%) | 48 (90.6%) | 14 (87.5%) | |
| Stage III | 3 (3.8%) | 0 (0.0%) | 2 (3.8%) | 1 (6.3%) | |
| Postoperative complication | 40 (25.5%) | 4 (12.5%) | 28 (27.7%) | 8 (33.3%) | 0.143 |
| Length of hospital stay (days) | 15.3±5.9 | 15.1±5.6 | 15.4±6.3 | 15.0±5.2 | 0.952 |
| Body mass index (kg/m2) | 23.4±3.1 | 26.1±2.9 | 23.1±2.7 | 21.0±2.7 | <0.001 |
| Preoperative Quality of life | 57.9±25.6 | 72.6±14.1 | 59.8±24.9 | 30.1±19.3 | <0.001 |
| Variables | Pathology | ||
|---|---|---|---|
|
|
|||
| Group A Non-malignancy (n=77) | Group B Malignancy (n=80) | P-value | |
| Age (years) | 57.9±13.3 | 62.8±10.0 | 0.010 |
| Sex | 0.122 | ||
| Male/Female | 47/30 | 39/41 | |
| Comorbidity: One or more | 43 (55.8%) | 51 (63.7%) | 0.312 |
| Previous Diabetes mellitus | 11 (14.3%) | 33 (41.3%) | <0.001 |
| Operation | 0.003 | ||
| PD* | 5 (6.5%) | 19 (23.8%) | |
| PPPD† | 72 (93.5%) | 61 (76.3%) | |
| Postoperative complication | 15 (19.5%) | 25 (31.3%) | 0.091 |
| Clavien-dindo classification | 0.505 | ||
| Grade II | 10 (66.7%) | 14 (56.0%) | |
| Grade ≥III | 5 (33.3%) | 11 (44.0%) | |
| Length of hospital stay | 15.1±6.1 | 15.4±5.9 | 0.737 |
| Body mass index (kg/m2) | 23.6±3.2 | 23.2±3.1 | 0.431 |
| Preoperative Quality of life | 66.0±21.3 | 50.2±27.2 | <0.001 |
| Preoperative nutritional status | 0.050 | ||
| Well-nourished | 21 (27.3%) | 11 (13.8%) | |
| At risk | 48 (62.3%) | 53 (66.3%) | |
| Malnourished | 8 (10.4%) | 16 (20.0%) | |
고 찰
- 1. Cameron JL, Riall TS, Coleman J, Belcher KA. One thousand consecutive pancreaticoduodenectomies. Ann Surg 2006;244:10-5. ArticlePubMedPMC
- 2. Winter JM, Cameron JL, Campbell KA, Arnold MA, Chang DC, Coleman J, et al. 1423 pancreaticoduodenectomies for pancreatic cancer:a single-institution experience. J Gastrointest Surg 2006;10:1199-210. ArticlePubMed
- 3. Greenblatt DY, Kelly KJ, Rajamanickam V, Wan Y, Hanson T, Rettammel R, et al. Preoperative factors predict perioperative morbidity and mortality after pancreaticoduodenectomy. Ann Surg Oncol 2011;18:2126-35. ArticlePubMedPDF
- 4. Lyu Y, Li T, Cheng Y, Wang B, Chen L, Zhao S. Pancreaticojejunostomy versus pancreaticogastrostomy after pancreaticoduodenectomy:an up-to-date meta-analysis of RCTs applying the ISGPS (2016) criteria. Surg Laparosc Endosc Percutan Tech 2018;28:139-46. ArticlePubMedPMC
- 5. Petzel MQB, Hoffman L. Nutrition implications for long-term survivors of pancreatic cancer surgery. Nutr Clin Pract 2017;32:588-98. ArticlePDF
- 6. La Torre M, Ziparo V, Nigri G, Cavallini M, Balducci G, Ramacciato G. Malnutrition and pancreatic surgery:prevalence and outcomes. J Surg Oncol 2013;107:702-8. ArticlePubMedPDF
- 7. Shinkawa H, Takemura S, Uenishi T, Sakae M, Ohata K, Urata Y, et al. Nutritional risk index as an independent predictive factor for the development of surgical site infection after pancreaticoduodenectomy. Surg Today 2013;43:276-83. ArticlePubMedPDF
- 8. Kim E, Kang JS, Han Y, Kim H, Kwon W, Kim JR, et al. Influence of preoperative nutritional status on clinical outcomes after pancreatoduodenectomy. HPB (Oxford) 2018;20:1051-61. ArticlePubMed
- 9. Callery MP, Pratt WB, Kent TS, Chaikof EL, Vollmer CM Jr. A prospectively validated clinical risk score accurately predicts pancreatic fistula after pancreatoduodenectomy. J Am Coll Surg 2013;216:1-14. ArticlePubMed
- 10. Probst P, Keller D, Steimer J, Gmür E, Haller A, Imoberdorf R, et al. Early combined parenteral and enteral nutrition for pancreaticoduodenectomy - retrospective cohort analysis. Ann Med Surg (Lond) 2016;4:68-73. Article
- 11. Karagianni VT, Papalois AE, Triantafillidis JK. Nutritional status and nutritional support before and after pancreatectomy for pancreatic cancer and chronic pancreatitis. Indian J Surg Oncol 2012;3:348-59. ArticlePubMedPMCPDF
- 12. Lis CG, Gupta D, Lammersfeld CA, Markman M, Vashi PG. Role of nutritional status in predicting quality of life outcomes in cancer--a systematic review of the epidemiological literature. Nutr J 2012;11:27.ArticlePubMedPMCPDF
- 13. Gupta D, Lammersfeld CA, Vashi PG, Dahlk SL, Lis CG. Can subjective global assessment of nutritional status predict survival in ovarian cancer? J Ovarian Res 2008;1:5.ArticlePubMedPMCPDF
- 14. Park JW, Jang JY, Kim EJ, Kang MJ, Kwon W, Chang YR, et al. Effects of pancreatectomy on nutritional state, pancreatic function and quality of life. Br J Surg 2013;100:1064-70. ArticlePubMedPDF
- 15. Phillips ME. Pancreatic exocrine insufficiency following pancreatic resection. Pancreatology 2015;15:449-55. ArticlePubMed
- 16. Matsumoto J, Traverso LW. Exocrine function following the whipple operation as assessed by stool elastase. J Gastrointest Surg 2006;10:1225-9. ArticlePubMed
- 17. Goess R, Ceyhan GO, Friess H. Pancreatic exocrine insufficiency after pancreatic surgery. Panminerva Med 2016;58:151-9. PubMed
- 18. Edge SB. American Joint Committee on Cancer (ACJJ). kAJCC cancer staging handbook:AJCC cancer staging manual. 7th ed. New York: Springer; 2010.
- 19. Clavien PA, Barkun J, de Oliveira ML, Vauthey JN, Dindo D, Schulick RD, et al. The Clavien-Dindo classification of surgical complications:five-year experience. Ann Surg 2009;250:187-96. PubMed
- 20. Guigoz Y. The Mini Nutritional Assessment (MNA) review of the literature--what does it tell us? J Nutr Health Aging 2006;10:466-85; discussion 485-7. PubMed
- 21. Park HK, Lim BK, Choi SH, Lee HR, Lee DS. Verification of the appropriateness when a shortened version of the Mini Nutritional Assessment (MNA) is applied for determining the malnutrition state of elderly patients. J Korean Soc Parenter Enter Nutr 2009;2:13-8. Article
- 22. Fitzsimmons D, Johnson CD, George S, Payne S, Sandberg AA, Bassi C, et al. Development of a disease specific quality of life (QoL) questionnaire module to supplement the EORTC core cancer QoL questionnaire, the QLQ-C30 in patients with pancreatic cancer. EORTC Study Group on quality of life. Eur J Cancer 1999;35:939-41. PubMed
- 23. Ozola Zalite I, Zykus R, Francisco Gonzalez M, Saygili F, Pukitis A, Gaujoux S, et al. Influence of cachexia and sarcopenia on survival in pancreatic ductal adenocarcinoma:a systematic review. Pancreatology 2015;15:19-24. ArticlePubMed
- 24. World Health Organization (WHO). Physical status:the use and interpretation of anthropometry. Report of a WHO Expert Committee. Geneva: WHO; 1995. Report No.:854.
- 25. Arvaniti M, Danias N, Theodosopoulou E, Smyrniotis V, Karaoglou M, Sarafis P. Quality of life variables assessment, before and after pancreatoduodenectomy (PD):prospective study. Glob J Health Sci 2015;17:203-10. ArticlePDF
- 26. van Dijk SM, Heerkens HD, Tseng DSJ, Intven M, Molenaar IQ, van Santvoort HC. Systematic review on the impact of pancreatoduodenectomy on quality of life in patients with pancreatic cancer. HPB (Oxford) 2018;20:204-15. ArticlePubMed
- 27. Hinz A, Singer S, Brahler E. European reference values for the quality of life questionnaire EORTC QLQ-C30:results of a German investigation and a summarizing analysis of six European general population normative studies. Acta Oncol 2014;53:958-65. ArticlePubMed
- 28. Bharadwaj S, Ginoya S, Tandon P, Gohel TD, Guirguis J, Vallabh H, et al. Malnutrition:laboratory markers vs nutritional assessment. Gastroenterol Rep (Oxf) 2016;4:272-80. ArticlePubMedPMC
- 29. Hendifar A, Osipov A, Khanuja J, Nissen N, Naziri J, Yang W, et al. Influence of body mass index and albumin on perioperative morbidity and clinical outcomes in resected pancreatic adenocarcinoma. PLoS One 2016;11:e0152172.ArticlePubMedPMC
References
Figure & Data
REFERENCES
Citations

- Factors Affecting Nutritional Index and Length of Stay in Pancreatic Cancer in the Older Adults
So Young Jun, Mo Na Choi, Joon Seong Park, Hyang Kyu Lee
Asian Oncology Nursing.2023; 23(3): 91. CrossRef
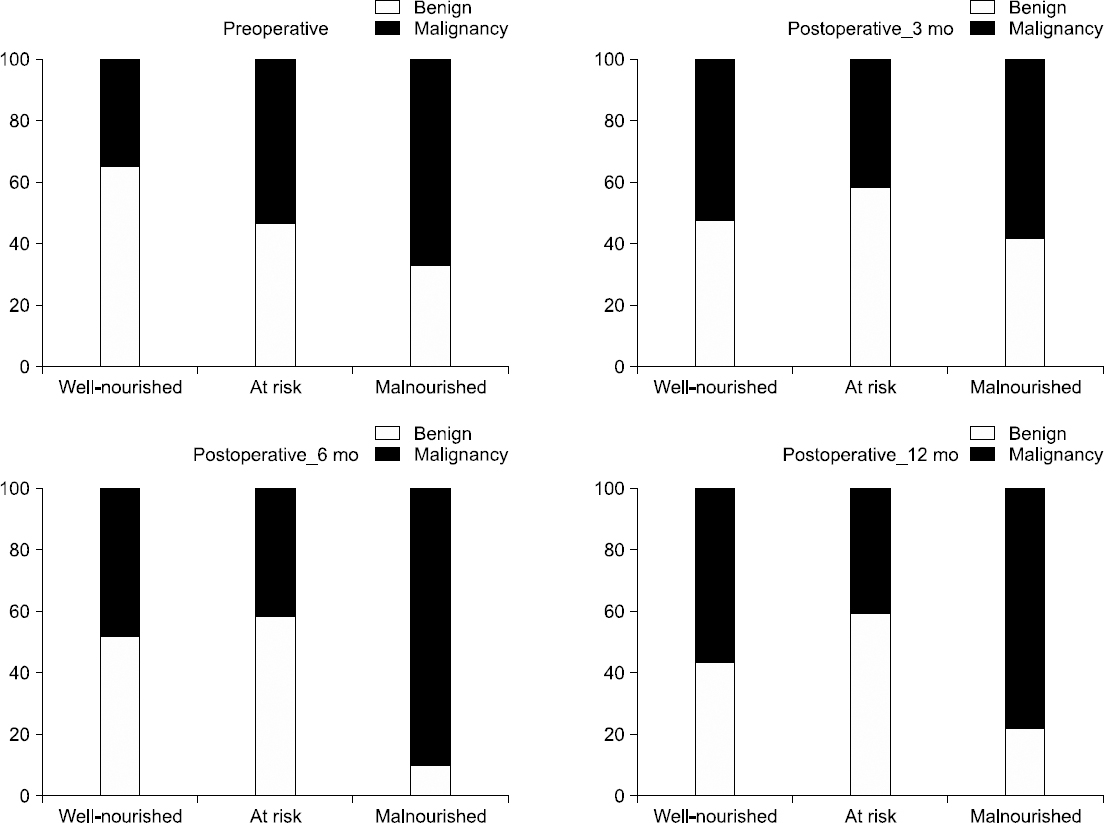
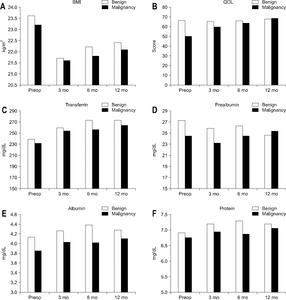
Fig. 1
Fig. 2
Characteristics according to preoperative nutritional status
| Variables | Overall n=157 | Well-nourished n=32 (20.4%) | At risk n=101 (64.3%) | Malnourished n=24 (15.3%) | P-valve |
|---|---|---|---|---|---|
| Age (years) | 60.4±11.9 | 58.3±13.1 | 60.5±10.6 | 62.5±15.5 | 0.433 |
| Sex | 0.183 | ||||
| Male/Female | 80/74 | 14/6 | 47/45 | 19/23 | |
| Comorbidity: One or more | 94 (59.9%) | 16 (17.0%) | 63 (67.0%) | 15 (16.0%) | 0.442 |
| Previous Diabetes mellitus | 44928.0%) | 5 (15.6%) | 32 (31.7%) | 7 (29.2%) | 0.210 |
| Operation | 0.783 | ||||
| PD |
24 (15.3%) | 6 (18.8%) | 14 (13.9%) | 4 (16.7%) | |
| PPPD |
133 (84.7%) | 26 (81.3%) | 87 (86.1%) | 20 (83.3%) | |
| Diagnosis | 0.050 | ||||
| Benign | 77 (49.0%) | 21 (65.6%) | 48 (47.5%) | 8 (33.3%) | |
| Malignancy | 80 (51.0%) | 11 (34.4%) | 53 (52.5%) | 16 (66.7%) | |
| Stage I | 8 (10.0%) | 4 (36.4%) | 3 (5.7%) | 1 (6.5%) | |
| Stage II | 69 (86.3%) | 7 (63.6%) | 48 (90.6%) | 14 (87.5%) | |
| Stage III | 3 (3.8%) | 0 (0.0%) | 2 (3.8%) | 1 (6.3%) | |
| Postoperative complication | 40 (25.5%) | 4 (12.5%) | 28 (27.7%) | 8 (33.3%) | 0.143 |
| Length of hospital stay (days) | 15.3±5.9 | 15.1±5.6 | 15.4±6.3 | 15.0±5.2 | 0.952 |
| Body mass index (kg/m2) | 23.4±3.1 | 26.1±2.9 | 23.1±2.7 | 21.0±2.7 | <0.001 |
| Preoperative Quality of life | 57.9±25.6 | 72.6±14.1 | 59.8±24.9 | 30.1±19.3 | <0.001 |
*PD = Pancreatoduodenectomy;
†PPPD = Pylorus preserving pancreatoduodenectomy.
Characteristics according to malignancy and non-malignancy
| Variables | Pathology | ||
|---|---|---|---|
| Group A Non-malignancy (n=77) | Group B Malignancy (n=80) | P-value | |
| Age (years) | 57.9±13.3 | 62.8±10.0 | 0.010 |
| Sex | 0.122 | ||
| Male/Female | 47/30 | 39/41 | |
| Comorbidity: One or more | 43 (55.8%) | 51 (63.7%) | 0.312 |
| Previous Diabetes mellitus | 11 (14.3%) | 33 (41.3%) | <0.001 |
| Operation | 0.003 | ||
| PD |
5 (6.5%) | 19 (23.8%) | |
| PPPD |
72 (93.5%) | 61 (76.3%) | |
| Postoperative complication | 15 (19.5%) | 25 (31.3%) | 0.091 |
| Clavien-dindo classification | 0.505 | ||
| Grade II | 10 (66.7%) | 14 (56.0%) | |
| Grade ≥III | 5 (33.3%) | 11 (44.0%) | |
| Length of hospital stay | 15.1±6.1 | 15.4±5.9 | 0.737 |
| Body mass index (kg/m2) | 23.6±3.2 | 23.2±3.1 | 0.431 |
| Preoperative Quality of life | 66.0±21.3 | 50.2±27.2 | <0.001 |
| Preoperative nutritional status | 0.050 | ||
| Well-nourished | 21 (27.3%) | 11 (13.8%) | |
| At risk | 48 (62.3%) | 53 (66.3%) | |
| Malnourished | 8 (10.4%) | 16 (20.0%) | |
*PD = Pancreatoduodenectomy;
†PPPD = Pylorus preserving pancreatoduodenectomy.
PD = Pancreatoduodenectomy; PPPD = Pylorus preserving pancreatoduodenectomy.
PD = Pancreatoduodenectomy; PPPD = Pylorus preserving pancreatoduodenectomy.

 E-submission
E-submission KSPEN
KSPEN KSSMN
KSSMN ASSMN
ASSMN JSSMN
JSSMN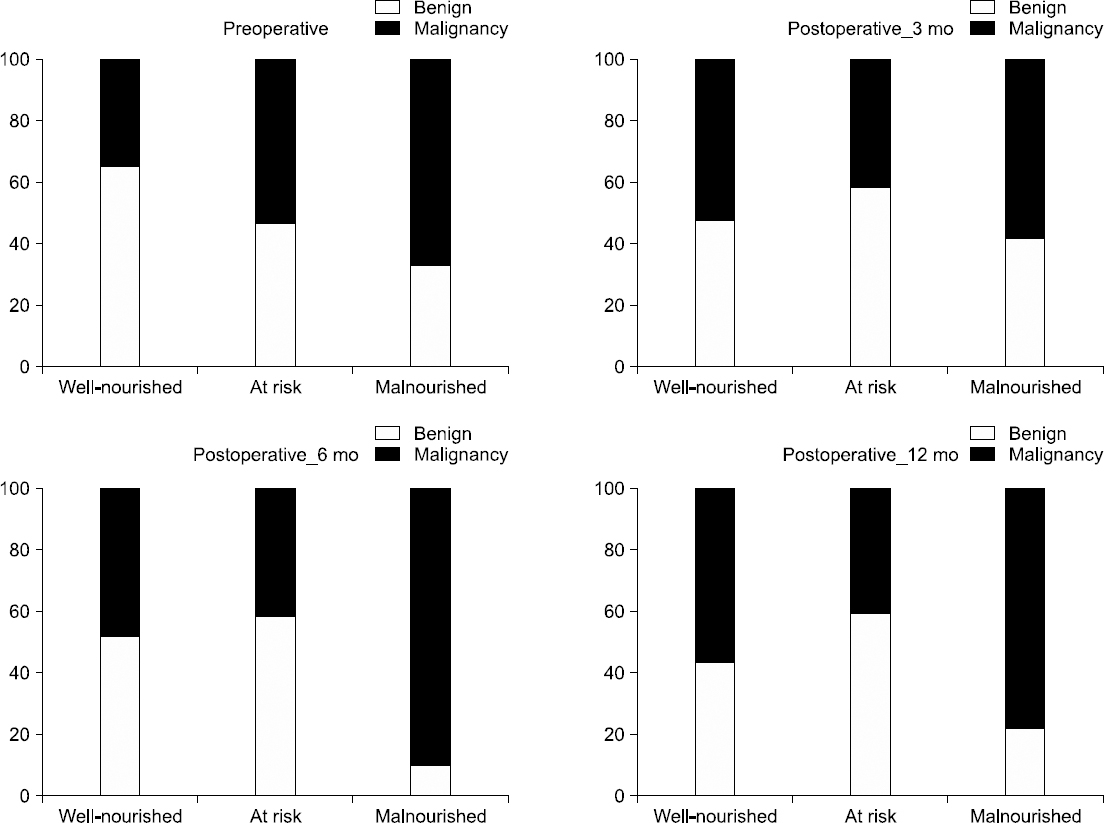
 Cite
Cite