Abstract
Refeeding syndrome refers to a life-threatening shift of electrolytes and fluid with metabolic abnormalities in malnourished patients undergoing refeeding, whether orally, enterally, or parenterally. Clinical findings are fluid-balance abnormalities, abnormal glucose metabolism, hypophosphatemia, hypomagnesemia, hypokalemia and deficiencies of vitamin and trace element. Multiple organ systems including cardiac, respiratory, neurologic, renal, hematologic, and gastrointestinal can be affected. When recognized in a timely manner, these complications can be easily and successfully prevented and treated. Four factors appear fundamental: early identification of patients at risk, correction of abnormalities before refeeding, close monitoring during refeeding, and an appropriate feeding regimen.
-
Keywords: Refeeding syndrome; Nutritional support; Prevention and control
서론
영양재개증후군(refeeding syndrome)은 제2차 세계대전 당시 필리핀에 일본군 죄수로 있던 미군 포로 등이 장기간의 굶주림 후 영양공급이 시작되었을 때 예상하지 못한 순환기계와 신경계 이상소견의 발생이 관찰되면서 알려지기 시작했다. 제2차 세계대전 당시에도 중부유럽 일부에서 기근과 굶주림이 있었지만 영양공급 부족과 재개에 의한 합병증인 부종에 대해서만 알려졌다.
1 영양재개증후군은 영양부족이나 영양실조 환자에서 정맥영양이나 경장영양뿐만 아니라 환자 스스로 입으로 음식물을 섭취하는 경우에도 발생할 수 있다. 수분과 전해질의 이상소견과 함께 대사이상도 발생하며 심부전, 부정맥, 경련, 빈혈 등 중대한 심혈관계, 신경계와 혈액이상 등을 유발하여 심한 경우 환자가 사망할 수도 있는 중대한 질환이다.
2
영양재개증후군의 대표적인 양상은 저인산혈증이며 수분과 염분의 균형 이상과 당, 단백, 지질의 대사 이상, 비타민 부족, 저칼륨혈증, 저마그네슘혈증 등이 발생하기도 한다. 그러나 이러한 중대한 이상 소견은 실제 임상에서 간과되기 쉬운데 특이 중환자실뿐만 아니라 일반병실에서도 진단지연으로 적절한 조치가 이루어지지 않는 경우들이 있다.
2 하지만 영양재개증후군의 정의가 합의된 것이 없어서 아직 실제적인 발생 빈도는 아직 명확히 알려지지 않았다. 그러나 대표적인 양상인 저인산혈증의 경우 심한 저인산혈증은 전제 입원환자의 0.43%에서 발생한다는 보고가 있으며, 중환자실 환자의 34%에서 영양재개 후 저인산혈증이 발생하는 등 영양재개증후군은 환자의 영양치료 중 결코 간과할 수 없는 질환이다.
3
이 글에서는 영양재개증후군의 발생기전, 임상양상, 위험군의 선별, 치료와 예방법을 살펴봄으로써 임상영양을 처음 접하는 의료진이 일정 이상의 굶주림 후 식이를 시작할 때 발생할 수 있는 치명적인 합병증에 대한 대처에 대해 논하고자 한다.
본론
1. 발생기전
금식이 시작되면 혈당은 단기간에 감소하지 않으며 혈중 인슐린 감소와 글루카곤 증가로 인해 24∼72시간 내에 감소가 시작된다. 혈당항상성의 유지는 뇌, 적혈구, 콩팥 수질 등 기관의 기능 유지에 필수적이기 때문이다. 이와 같은 변화로 인하여 간에서의 당원분해가 증가하고 체내 지방의 중성지방 지방분해가 자극되어 지방산과 글리세롤의 생성이 증가하는데, 이들은 조직의 에너지로 사용되거나 간에서 케톤체로 변환된다. 이후 체내의 글리코겐을 모두 소모하게 되면 간에서 당신생이 증가하게 되며, 이때 근육의 파괴로 얻어진 아미노산과 젖산과 글리세롤 등을 이용하여 뇌와 적혈구에서 사용해야 할 당을 생성한다. 이와 같이 금식 기간에는 사용하는 에너지원의 사용 경로가 탄수화물에서 단백질과 지질로 바뀌게 되고 동시에 기초대사량의 20%∼25% 정도가 감소한다. 금식이 지속되면 체내의 근육과 단백질의 소실을 막기 위해 조직은 주요 에너지원으로 사용하던 케톤체와 지방산의 사용을 줄이고 혈중 케톤체가 증가하면 뇌에서의 주요 에너지원이 당에서 케톤체로 변환된다. 뇌에서의 당 요구량이 감소하게 되면 간에서의 당신생이 감소하여 아미노산의 근원인 근육을 보존할 수 있게 된다. 또한 세포 내 미네랄들의 부족이 발생하게 되는데 일정기간 동안 미네랄의 농도가 정상 범위인 경우도 있다.
영양분이 다시 공급되면 경구나 정맥으로 투여된 당은 혈당을 상승시켜 인슐린의 분비를 자극하고 글루카곤의 분비를 감소시킨다. 이로 인하여 글리코겐, 지질, 단백의 합성의 변화가 발생하고 동화상태를 유지하기 위해서 인, 마그네슘 등의 미네랄과 티아민 등의 조효소의 요구량이 증가하게 된다. 인슐린은 칼륨과 마그네슘, 인의 세포 안으로의 이동을 유발하는데, 이로 인하여 이 성분들의 세포 외 농도들이 급격하게 감소하게 된다. 또한 섭취한 당은 콩팥에서의 수분과 염분배출을 감소시켜서 소변량이 일정이상 유지되더라도 체액량 과잉이 발생할 수 있다.
2-5 이와 같이 영양재개증후군의 주요 병태생리는 저인산혈증, 저마그네슘혈증, 저칼륨혈증, 수분대사의 이상, 당대사의 이상, 티아민 등의 비타민 부족 등이다.
영양재개증후군은 아직 명확한 정의가 합의된 것이 없기 때문에, 정확한 발생빈도에 대해서는 아직 잘 알려지지 않았다. 많은 연구들에서 전해질, 미네랄, 비타민 등 혈액검사 이상에서부터 심혈관계와 신경계 이상 소견까지 여러 가지 진단 기준으로 영양재개증후군을 판단하고 있어 다양한 연구결과가 보고되고 있다.
1-5 그러나 영양재개증후군의 대표적인 소견인 저인산혈증은 대부분의 연구자들이 진단기준으로 인정하고 있다. 일만 명이 넘는 병원입원환자를 대상으로 한 연구에서는 0.43%에서 심각한 저인산혈증이 관찰되었고, 이 환자에서 사망률이 높았다. 또한 알코올 중독자, 패혈증, 당뇨병성 케톤산혈증과 특히 영양실조 환자에서 영양재개증후군 발생 위험이 높았다.
6 인 보충 치료를 받았던 62명의 중환자를 대상으로 한 연구에서는 34%에서 영양재개증후군에 의한 저인산혈증이 관찰되었고 인공호흡 치료와 입원 기간 증가의 연관성이 있었다.
7 2010년 영국에서 발표된 National Confidential Enquiry into Patient Outcome and Death of the United Kingdom에서는 3개월간 정맥영양치료를 받았던 887명 환자의 39.3%에서 대사성 이상이 발생하였으며 저인산혈증(13.3%), 저칼륨혈증(8%), 저마그네슘혈증(7%)이 관찰되었다. 또한 이 연구에서 의무기록 조사로 전체 대상환자 중 60%에서 영양재개증후군의 위험성이 있었다고 판단하였다. 그러나 이 환자들 중 50%에서 담당 의료진이 영양재개증후군의 위험성을 인지하고 있었으며 14%에서 영양재개증후군이 발생했다고 보고하였다.
3
최근 보고된 경장영양이나 정맥영양 치료를 받는 243명의 환자를 대상으로 한 전향적 연구에서는 영양재개증후군의 위험성이 있는 환자에서 엄격한 영양재개증후군의 진단기준을 적용했다. 혈청 칼륨 2.5 mmol/L 미만, 혈청 인 0.5 mmol/L 미만, 혈청 마그네슘 0.5 mmol/L 미만이면서 부종이나 급성 체내 수분 과잉이 동반되고 호흡부전이나 심장부전, 폐부종 등의 장기기능이상 동반되어 있는 경우에만 영양재개증후군으로 정의했다. 이 연구에서는 2%의 환자가 영양재개증후군으로 진단되었고 저마그네슘혈증이 영양재개증후군의 위험인자였으나 환자의 사망과는 연관성이 없었다.
8 단일 의료기관에서 입원환자를 18개월 동안 관찰한 연구에서는 45,000명이 넘는 대상자 중 2%에서 0.5 mmol/L 이하의 저인산혈증이 관찰되었으며 이 중 30%가 입원 치료 중 사망하였으며, 사망환자의 10%가 영양재개증후군에 의해서 발생하였다.
9 이와 같이 아직 명확히 확립되지 않는 영양재개증후군의 정의 등 연구와 조사에 많은 제한이 있어 영양재개증후군의 발생빈도와 중요성에 대해 다양한 보고들과 분석들이 있지만, 대부분의 보고들에서 심한 경우 환자가 사망할 수도 있는 중요한 질환이라는 것에 대해서는 동의하고 있다.
영양재개증후군의 증상은 매우 다양하고 예고 없이 발생할 수도 있으며 영양 공급 시작 시기가 아닌 시간이 경과한 상태에서도 발생하는 경우가 있어 매우 주의가 필요하다. 영양재개증후군의 증상은 전해질 대사 이상으로 인한 신경계, 순환기계, 골격근 기능 이상 등으로 발생하는데 다양한 형태와 중증도를 보인다. 경한 혈청 전해질 이상에서는 특이 증상이 없으나 갑자기 발생하여 발생원인에 대한 적절한 평가와 신속한 조치가 어려운 경우도 있다. 영양재개증후군의 증상은 욕지기, 구토, 졸음과 같은 경미한 것부터 호흡부전, 심장부전, 저혈압, 부정맥, 섬망, 혼수 그리고 사망까지 매우 다양하며 원인에 따라 특징적인 소견이 관찰된다(
Table 1).
3,5,10
Table 1Clinical manifestations of refeeding syndrome
3-5
|
System |
Clinical manifestations |
|
Cardiovascular |
Sudden death, arrhythmias, hypertension, congestive heart failure, cardiomyopahty, shock, death |
|
Respiratory |
Dyspnea, hypoventilation, respiratory failure, ventilator dependency, diaphragm weakness, intercostal muscle weakness, pulmonary edema |
|
Neurologic |
Weakness, parasthesias, tremors, ataxia, delirium, acute encephalopathy, coma, Guillan-Barre-like syndrome, central pontine myelinolysis, Wernicke's encephalopathy, Korsakoff's psychosis |
|
Musculoskeletal |
Weakness, fatigue, muscle cramps, myalgia, rhabdomyolysis, osteomalacia |
|
Gastrointestinal and hepatic |
Anorexia, abdominal pain, diarrhea, constipation, vomiting, loss of appetite, paralytic ileus, hepatic failure |
|
Metabolic |
Metabolic alkalosis, metabolic acidosis, respiratory alkalosis, hyperglycemia, insulin resistance, tetany, osteomalacia |
|
Hematologic |
Infections, thrombocytopenia, hemolysis, anemia |
|
Renal |
Acute tubular necrosis, renal failure |
1) 저인산혈증
저인산혈증은 영양재개증후군의 대표적인 소견이다. 인은 신체에서 칼슘 다음으로 많이 함유하고 있는 무기질로 체내 보유량은 500∼800 g 정도로 80%는 칼슘과 결합하여 골격계를 구성하고 있고 나머지 20%는 연조직과 근육에 존재한다. 매일 음식을 통해 1 g 정도의 인이 섭취되는데 80%는 공장에서 흡수되고 정상적인 식사로 섭취한 인의 50%∼70% 정도가 흡수되지만 섭취량이 낮을 때에는 90%까지 흡수된다. 인은 시리얼이나 땅콩과 같은 단백질이 풍부한 음식에 많고 일반적으로 섭취 부족은 드물며 오히려 과다 섭취를 하는 경우가 많다. 인의 배설은 주로 콩팥에서 이루어지며 90%가 배설되는데 사구체에 의해 걸러진 인은 근위 세뇨관에서 흡수되어 항상성을 유지하게 되며 10%는 장관을 통해 소실된다. 인은 세포 내 주요 음이온으로 탄수화물이나 지질의 섭취와 산염기 균형의 변화에 의해 세포내외를 자유롭게 이동하는데 산성 환경에서는 인이 세포 안에서 혈장으로 이동한다.
2
인은 뼈와 치아 등 골격조직을 구성하는 주요 성분이며 체내의 유전정보를 전달하는 DNA와 RNA의 구성성분으로 세포 성장에 필수적이다. 또한 세포막의 인지질 성분으로 영양소를 세포내외로 운반하는 조절작용을 하기도 한다. DNA와 RNA의 합성, adenosine triphosphate (ATP)와 adenosine diphosphate 등 에너지 생성과 저장 과정, 단백질, 지질, 탄수화물 대사에도 관여한다. 세포 내 완충에 중요한 역할을 하고 소변 내 수소 이온 완충에 필수적으로 신체의 정상 산도의 유지에 중요한 역할을 하고 있다. 또한 해당작용과 산화적 인산화 등 세포 대사 경로, 단백 인산화 등 많은 효소반응에서 중요한 조절 작용 등을 한다. 해당작용의 부산물인 2,3-diphosphoglycerate (DPG)는 적혈구내의 혈색소에의 산소 해리를 조절하고 흥분-자극 반응과 신경계 전도에도 관여한다. 백혈구의 화학쏠림성(chemotaxis), 포식작용(phagocytosis), 혈소판의 응혈뒤당김(clot retraction)에도 작용한다.
2,4
인은 인체 내에서 여러 작용을 하기 때문에 부족이 발생하면 다양한 임상양상이 발생할 수 있다. 심장 근육병증이 발생하여 심부전, 부정맥, 저혈압, 심근병증, 쇼크, 사망이 발생한다. 대사성 산증과 신세뇨관 이상을 유발하거나 횡문근용해증에 의해 급성세뇨관 괴사가 유발된다. 횡경막 기능약화로 인공호흡기 이탈 장해가 발생하고 근육통이 발생한다. 신경계도 영향을 받아 경련, 불안한 정신상태, 감각 이상, 혼수 상태를 보인다. 심한 저인산혈증은 혈소판 감소증, 혈액 응고 이상, 백혈구의 대식작용과 화학쏠림성 감소시키고 적혈구의 2,3-DPG의 감소로 용혈과 조직으로의 산소 공급 감소가 발생한다.
2-4
혈청 무기인 수치가 1.0 mg/dL 이하인 심한 저인산혈증이 발생하면 다양한 임상양상이 발생할 수 있는데 실제적으로 심한 저인산혈증은 자주 관찰되지는 않으며 대부분의 경우는 중요한 임상 양상이 동반되지 않는다.
11 하지만 총정맥영양치료에 의한 저인산혈증으로 사망한 예도 있으며 영양재개증후군에 의한 심한 저인산혈증은 이환율을 증가시킨다.
12,13
2) 저마그네슘혈증
마그네슘은 60%가 칼슘, 인과 함께 골격을 구성하고 있으며 근육과 간의 연조직에 분포하고 있다. 또한 탄수화물, 단백질, 지질과 핵산의 대사 과정에 관여하는 효소 활성화의 중요한 조효소로 산화적 인산화 반응에서 ATP의 합성과 에너지 생성에 중요한 조효소로 작용한다. 또한 아세틸콜린의 분비 감소에 의한 신경계 안정과 근육 이완 작용으로 칼슘과 반대적인 역할을 해서 마그네슘의 부족으로 심장기능이상이나 신경과 근육계 합병증이 발생한다. 섭취한 마그네슘의 30%∼40%만 흡수되고 나머지는 대변으로 배설되고 체내의 마그네슘은 신장으로 배설되는데 칼슘과 달리 비타민 D의 영향을 받지 않는다.
14 영양재개증후군에서 저마그네슘혈증 발생의 기전은 아직 명확하게 밝혀지지 않았으나 고탄수화물 식이와 마그네슘이 부족한 식이, 세포 내로의 마그네슘 이동이 원인으로 제시되고 있다. 또한 영양공급 전 마그네슘의 부족은 저칼륨혈증이나 저칼슘혈증을 악화시킨다. 저마그네슘혈증의 대부분은 심각한 임상양상을 보이지 않으나 0.5 mmol/L의 심각한 저마그네슘혈증에서는 경련, 감각이상, 강직증, 경련, 흥분, 혼돈, 운동실조 등 신경학적 증상이 나타난다. 부정맥과 고혈압, 복통과 식욕부진도 발생한다.
15
3) 저칼륨혈증
칼륨은 세포내액의 주요 양이온으로 체액의 삼투압과 수분 균형을 조절하고 산염기 균형에도 관여한다. 신경과 근육의 흥분, 근육의 수축과 이완작용, 신경의 자극전달, 췌장에서의 인슐린 공급, 글리코겐 및 단백질 합성에서 중요한 역할을 한다. 섭취한 칼륨의 90%는 소장에서 단순확산에 의해 쉽게 흡수되며 대부분이 세포 내액에 존재한다. 체내 칼륨의 총량은 콩팥에 의해 조절되는데 알도스테론, 알칼리증, 식이 내 칼륨 등이 영향을 미친다. 영양부족으로 체내의 칼륨이 많이 부족하더라고 혈청 내 칼륨 농도는 정상인 경우가 많으며, 다시 영양이 공급되었을 때 인슐린에 의해 혈청 내 칼륨이 세포 내로 이동하게 되어 저칼륨혈증이 발생한다.
2,4
저칼륨혈증의 임상양상은 매우 다양하며 부정맥, 저혈압, 심정지 등의 심혈관계 증상과 마비성 장폐색과 변비, 설사, 욕지기, 구토, 식욕부진 등의 소화기 증상이 나타나며 쇠약, 마비, 혼동, 횡문근융해증, 호흡저하 및 곤란 등의 신경근육성 소견이 나타날 수 있다. 또한 디지탈리스 독성, 내당능장애를 증가시키고 간성뇌증을 악화시킨다. 저칼륨혈증의 증상은 저인산혈증이나 저마그네슘혈증과 같이 혈청 농도 3.0 mmol/L이하의 심한 저칼륨혈증에서 임상증상이 나타난다.
2
4) 비타민 부족
장기간의 영양공급 부족은 심각한 비타민 결핍을 유발할 수 있으나 영양재개증후군에서의 비타민 부족의 임상양상은 주로 비타민 B1, 티아민 부족에 의한 것이다.
16,17 티아민 결핍에 의해 발생하는 급성질환은 급성정신혼돈, 조화운동못함증, 눈근육마비 등을 특징으로 하는 베르니케 뇌병증(Wernicke encephalopathy)이며, 티아민 결핍을 적절하게 치료하지 못했을 때 선행성 기억상실, 후행성기억상실, 작화증, 무감동증 등의 임상양상을 특징으로 하는 코르사노프 증후군(Korsakoff syndrome)이 발생한다. 베르니케 뇌병증은 비교적 국내에서도 많이 보고되고 있는 영양재개증후군의 형태로 기아, 신경성 식욕부진, 알코올중독, 암, 신장투석, 갑상선중독증, 흡수장애, 임신입덧, 장기간의 정맥영양치료 등에서 발생한다.
16,17 체내에 축적된 티아민이 고갈되거나 상당히 부족한 상태에서 탄수화물이 풍부한 음식을 섭취하거나 정맥 내로 포도당이 급속히 투입되면 다양한 효소 반응의 조효소인 티아민의 세포 내 사용량이 증가하고 혈액 내 티아민 부족으로 이어진다. 베르니케 뇌병증은 초기 급성 신경질환일 때 조기에 진단하고 치료하면 좋은 예후를 보이나, 그렇지 않으면 사망률이 17%∼20% 정도에 이를 수 있는 응급 질환이다.
16,17
베르니케 뇌병증의 위험인자가 있는 환자에서 급성정신혼돈, 조화운동못함증, 눈근육마비 등의 전형적인 증상이 있을 때 의심해야 하며 수평안구진탕을 보이기도 하고 티아민 정주 후 회복되면 진단할 수 있다. 베르니케 뇌병증의 영상진단방법으로 뇌전산단층촬영은 다른 뇌질환의 감별에만 도움이 되며 뇌자기공명영상이 진단에 도움을 준다. 양측 시상 내측의 고신호강도와 유두체의 위축, 시상 내측핵 위축으로 인한 제3뇌실의 확장 소견이 관찰되며 민감도 53%이고 특이도 93%로 정상소견이 관찰될 수도 있다.
18
5) 체내 수분 분포 이상
탄수화물에 의한 영양재개는 콩팥에서의 수분과 염분의 배출을 감소시켜 소변량이 정상인 경우에도 세포 외액과 체중증가를 유발하며, 특히 식사 중 염분의 양이 많을 수록 심해진다. 이와 같이 발생한 체내 수분 분포 이상은 심장부전, 탈수나 수분과다, 저혈압, 급성신부전, 폐부종, 호흡부전, 사망을 유발할 수 있다. 장기간 기아로 인해 심장근육 소실이 동반되는 경우 심혈관계 합병증 발생 위험성은 증가한다. 단백이나 지질을 주 영양성분으로 하는 영양재개는 체중감소와 소변에서의 염분배출을 유발하여 체내의 염분량이 감소하고, 고 단백질식이를 시행하는 경우 고장성 탈수증, 질소혈증, 대사성 산증을 동반한 고나트륨혈증이 발생할 수 있다.
19
6) 당대사의 이상
금식이 끝나고 당의 섭취가 시작되면 인슐린 분비와 글루카곤 분비 억제에 의해 당신생이 억제되고 아미노산 소비가 감소되어 음성 질소 균형이 호전된다. 그러나 억제된 당신생에 의해 계속 많은 양의 당이 공급되었을 때 고혈당이 발생하여 고삼투성 비케톤성 혼수, 케톤산혈증, 대사성 산증, 삼투성 이뇨, 탈수 현상이 발생할 수 있다. 또한 당은 지방으로 변환되어 고중성지방혈증이나 간기능 이상을 초래하며 높은 호흡률을 보여 이산화탄소 생성 증가와 고탄산혈증, 호흡부전을 유발하기 때문에 지방의 과량 투여를 주의하여야 한다.
20
영양재개증후군은 모든 환자에서 발생하는 것은 아니므로 영양재개증후군이 발생할 수 있는 상황을 우선 인지하여 발생을 최소화하는 것이 매우 중요하다. 진료초기부터 발생 위험성이 높은 대상자를 선별하여 감시하고 이상소견을 조기 진단하여 치료해야 한다. 또한 의사, 간호사, 영양사, 약사 등으로 구성된 영양지원팀과 같은 병원 내 관련 조직이 영양재개증후군의 인지와 교육, 치료에 적극적으로 참여해야 하며 이런 조직 구성원간의 적절한 의사전달과 환자의 영향상태 조절에 대한 다각적인 접근이 필요하다.
영양재개증후군의 발생 위험성이 높은 환자군에 대해서는 다양한 보고들이 있는데 대표적인 질환으로는 신경성 식욕부진, 만성알코올 중독, 암환자, 수술 후 환자, 질환을 동반한 노인환자, 만성적인 영양부족증, 특히 최근 일주일 이상 극심한 스트레스에 노출된 환자 등이며 이외에 다양한 질환에서 영양재개증후군의 발생 위험도가 증가한다(
Table 2).
2-5,10
Table 2Patient at risk of developing refeeding syndrome
|
Anorexia nervosa |
|
Chronic alcoholism |
|
Oncology patients |
|
Postoperative patients |
|
Elderly patients with comorbidities or decreased physiological reserve |
|
Poorly uncontrolled diabetes mellitus with electrolyte depletion |
|
Chronic malnutrition |
|
Marasmus/kwashiorkor |
|
Prolonged fasting/hypocaloric feeding |
|
Morbid obesity with profound weight loss |
|
High stress patient unfed for >7 days |
|
Malabsorptive syndrome such as inflammatory bowel disease, chronic pancreatitis, cystic fibrosis and short bowel syndrome |
|
Radiation therapy |
|
Stroke (neurological problems) |
|
Acquired immunodeficiency syndrome |
|
Long term antacid users (magnesium/aluminium salts bind phosphate) |
|
Electrolyte imbalance such as chronic diuretic users (loss of electrolytes) |
|
Institutionalized patients |
|
Pathological weight loss hunger strikes |
|
Poor social circumstance |
영양재개증후군의 발생 위험성이 높은 환자에서의 선별에 사용하는 기준에는 영국에서 2006년 National Institute for Clinical Excellence (NICE)에서 발표한 기준이 있다. 이 기준에서는 환자의 체질량지수, 체중감소, 식사량, 혈청 칼륨, 인, 마그네슘 수치와 음주력과 약물 복용력으로 위험군을 선정한다(
Table 3).
3,4,21
Table 3Criteria for determining people at high risk of developing refeeding syndrome (according to National Institute for Health and Clinical Excellence Guidelines)
3,4,21
|
The patient has one or more of the following: |
|
Body mass index less than 16 kg/m2
|
|
Unintentional weight loss greater than 15% within the last 3∼6 months |
|
Little or no nutritional intake for more than 10 days |
|
Low levels of potassium, phosphate or magnesium prior to feeding |
|
Or the patient has two or more of the following: |
|
Body mass index less than 18.5 kg/m2
|
|
Unintentional weight loss greater than 10% within the last 3∼6 months |
|
Little or no nutritional intake for more than 5 days |
|
A history of alcohol abuse or drugs including insulin, chemotherapy, antacids or diuretics |
5. 치료와 예방
1) 영양공급 전 이상 교정
영양재개증후군의 위험군이 선별이 되면 전해질 이상, 비타민 결핍, 체내 수분 이상 상태 등을 영양 공급 이전에 교정하는 것이 중요하다. 저인산혈증은 경증에서는 치료를 하지 않는 경우가 있으나 영양재개증후군의 위험성이 높은 환자에서는 혈청인의 수치가 정상범위보다 낮은 경우 영양재개 시작 전에 경구나 정맥으로 인을 보충하는 것이 권장된다. 1.6 mg/dL 이하인 심한 저인산혈증이거나 저인산혈증의 연관 증상이 보이면 반드시 인 보충 치료를 시행해야 한다.
2 신기능이 감소된 경우에는 인의 투여량을 절반으로 줄여야 하고 저칼슘혈증 등에 의한 신경학적 증상 발생 등을 관찰하면서 주의 깊게 투여하여야 한다. 환자의 혈청 칼륨치가 낮으면 potassium phosphate 제제를 사용하고 칼륨치가 높으면 sodium phosphate 제제를 사용한다. 인은 주사요법 시 반드시 생리식염수나 포도당에 희석하여 7.5 mmol/L 이하의 속도로 투여해야 한다.
3-5,22
저마그네슘혈증은 경증의 경우에는 산화마그네슘, 구연산마그네슘 등의 경구용 제제로 치료할 수 있으나 설사 등의 부작용이 발생하기도 한다. 혈청 마그네슘 농도가 1.2 mg/dL 미만인 심한 경우에도 증상이 없으면 경구용 제제로 치료할 수 있으나 저마그네슘혈증의 증상이 동반되면 황산마그네슘을 정맥으로 투여한다. 생리식염수나 포도당 수액에 혼합하여 시간당 1 g 이하의 속도로 3∼7일까지 투여할 수 있으며 매일 혈청 마그네슘 농도를 측정하여 과다 투여되지 않도록 주의하여야 한다. 또한 마그네슘의 투여는 저칼슘혈증과 저칼륨혈증을 회복시키므로 혈청 내 칼륨과 칼슘을 투여와 동시에 측정해야 한다.
3-5
저칼륨혈증은 혈청칼륨 농도가 3.5 m Eg/L 이하인 경우로 부정맥, 호흡부전 등의 생명에 지장을 주는 합병증을 예방하기 위해 치료를 해야 한다. 정맥으로 많은 양의 칼륨을 단기간에 투여하기 어렵기 때문에 경구 투여를 하기도 하지만 연관증상이 있거나 심한 저칼륨혈증에서는 정맥투여를 시행한다. 말초 정맥으로는 40 mEq/L, 중심정맥으로는 120 mEq/L의 농도로 20 mEq/h 이하의 속도로 수액에 혼합하여 투여한다. 고칼륨혈증 발생을 예방하기 위해 혈청 칼륨 농도를 측정해야 하고 심전도 검사 등으로 부정맥 발생을 감시해야 한다.
3-5
2) 모니터링
영양재개를 시작하면 영양재개증후군의 발생을 조기 진단하기 위해서 영양치료와 연관된 임상적인 소견과 혈액검사 소견의 변화에 대한 지속적인 감시가 필요하다. 체내 수분 과잉이나 폐부종, 울혈성심부전 등을 예방하기 위해 활력징후, 체중변화와 소변량 등을 측정해야 한다. 영양재개 첫 주 동안이나 임상적으로 안정화될 때까지 매일 혈청 전해질 검사를 실시하여야 한다. 혈당은 하루에 최소 1∼2회 측정하여 고혈당이나 저혈당을 예방하고 혈당이 100∼150 mg/dL로 유지하게 한다. 중환자에서 프리알부민(prealbumin) 수치는 저인산혈증을 예상할 수 있으며 온혈구검사, 간기능 검사도 매일 실시해야 한다. 중환자에서는 검사 빈도를 늘려야 하며 특히 영양재개에 의한 심장합병증은 영양공급 시작 일주일 내에 많이 발생하므로 이 기간 동안 혈압, 맥박, 심전도 변화, 수분균형 등을 반드시 지속적으로 확인해야 한다(
Table 4).
2-5,10,23
Table 4Daily monitoring patients at risk of developing refeeding syndrome
|
Clinical monitoring |
|
Nutrient intake (oral, enteral, parenteral) |
|
Body weight change |
|
Vital signs (pulse rate, blood pressure) |
|
Fluid intake and output |
|
Clinical manifestations (edema, neurologic signs and symptoms) |
|
Biochemical monitoring |
|
Plasma electrolytes (sodium, potassium, phosphate, magnesium, calcium) |
|
Blood urea nitrogen, creatinine |
|
Plasma glucose |
|
Blood gases |
|
Liver function test |
|
Electrocardiographic monitoring in severe cases |
|
Complete blood cell counts |
3) 영양공급
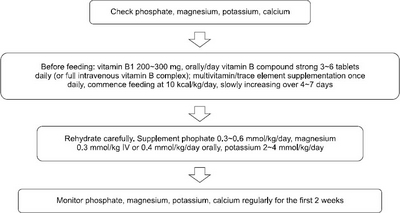
영양재개 증후군 위험군에서 예방하기 위한 적절한 영양공급방법에 대해서는 다양한 방법들이 제시되고 있다. NICE에서 제시한 가이드라인에 의하면 우선 인, 마그네슘, 칼륨, 칼슘 등의 전해질을 측정한 후에 티아민을 비롯한 비타민 B를 보충하고 10 kcal/kg/day의 열량으로 영양분을 공급한다. 영양 공급은 4∼7일에 걸쳐 목표만큼 증량하고 전해질과 미량원소를 지속 공급하면서 수분도 공급한다. 전해질은 영양공급 2주까지 계속 측정해서 이상소견이 관찰되면 교정한다(
Fig. 1).
3,4,21
Fig. 1Guidelines for management of patients at risk of refeeding syndrome. Adapted from National Institute for Clinical Excellence.
다른 문헌들에서는 영양공급 시작 단계에서는 필요한 열량의 20% 이상을 투여하지 않고 10 kcal/kg/day로 열량공급을 시작하지만 체질량지수가 14 kg/m
2 미만이거나 금식시간이 15일 이상 되는 환자에서는 5 kcal/kg/day의 열량공급을 권장하고 있다.
3,4 공급하는 열량은 환자의 임상증상과 혈액검사 소견을 관찰하면서 5 kcal/kg/day씩 증량하여 영양공급 7∼10일까지 20∼30 kcal/kg/day까지 서서히 증량한다. 공급 영양의 구성은 다양한 의견들이 있으나 최근 탄수화물 50∼60%, 지방 15∼25%, 단백질 20∼30%가 권장되고 있다.
수분의 공급은 20∼30 mL/kg/day의 용량으로 환자의 상태에 따라 조절하며 체내 수분 과다와 부족이 발생하지 않도록 한다. 경한 저나트륨혈증은 수분제한으로 조절할 수 있으나 증상을 동반하는 경우에는 생리식염수나 고장성식염수를 투여해야 한다. 전해질은 영양공급 개시 전 이상소견을 교정해야 하며 또한 이상소견이 없더라도 유지용량은 공급해야 한다(
Fig. 1). 비타민은 영양공급 전 부족증 유무를 떠나 티아민 200∼300 mg을 정맥으로 투여하고, 최소한 3일 동안은 매일 100∼300 mg을 경구나 정맥으로 지속 투여해야 하고 비타민 복합제제를 매일 경구로 3∼6정 투여하거나 정맥투여 한다. 셀레늄, 아연, 철분 등 미량원소도 필요에 따라 투여할 수 있다.
2-5,10
그러나 영양재개증후군을 예방하기 위해 NICE 가이드라인에서 제시하고 있는 영양 공급 초기에 적은 양으로 공급하면서 서서히 증량하는 방법은 저영양공급으로 회복 지연과 이환율 증가의 위험성이 있다는 주장도 있다. NICE 가이드라인 제정 전에는 일부 연구자들이 20 kcal/kg/day나 필요열량 50% 정도의 공급을 주장하기도 했으며 심한 거식증 환자를 대상으로 한 연구에서는 40 kcal/kg/day로 영양공급을 하여도 영양재개 증후군이 발생하지 않았다. 영양공급원으로 당원보다는 지질 공급을 확대하여 영양재개 초기부터 영양재개증후군 발생을 억제하면서 적절한 영양 공급을 제안하는 연구자도 있다. 그러나 아직 영양재개증후군에 대한 무작위 대조군 연구가 부족하여 NICE 가이드라인의 변경을 명확히 제시할 만한 연구결과는 보고되지 않았다.
24
결론
영양재개증후군은 영양부족이나 영양실조 환자에서 정맥영양이나 경장영양 이외에 환자 스스로 입으로 음식물을 섭취하는 경우에도 발생할 수 있는 질환이다. 발생빈도와 중요성에 대해 다양한 보고들이 있지만 심한 경우 환자가 사망할 수도 있는 중요한 질환이다. 대표적인 양상은 저인산혈증이며 수분과 염분의 균형 이상과 당, 단백, 지질의 대사 이상, 비타민부족, 저칼륨혈증, 저마그네슘혈증 등이 발생한다. 심혈관계, 호흡기계, 신경계, 콩팥, 소화기계와 혈액계 등의 이상을 유발하여 심한 경우 환자가 사망할 수도 있는 중대한 질환이다. 영양재개증후군은 적절한 시기에 진단하면 적절하게 예방과 치료를 할 수 있다. 이를 위해서는 위험군의 조기선별, 영양 전 이상소견 교정, 영양 치료 중 감시 그리고 적절한 식이 방법이 중요하다.
Conflict of interest: None.
References
- 1. Schnitker MA, Mattman PE, Bliss TL. A clinical study of malnutrition in Japanese prisoners of war. Ann Intern Med 1951;35(1):69-96. ArticlePubMedPDF
- 2. Crook MA, Hally V, Panteli JV. The importance of the refeeding syndrome. Nutrition 2001;17(7-8):632-7. ArticlePubMed
- 3. Walmsley RS. Refeeding syndrome: Screening, incidence, and treatment during parenteral nutrition. J Gastroenterol Hepatol 2013;28(Suppl 4):113-7. ArticlePubMedPDF
- 4. Mehanna H, Nankivell PC, Moledina J, Travis J. Refeeding syndrome--awareness, prevention and management. Head Neck Oncol 2009;1:4.ArticlePubMedPMCPDF
- 5. Boateng AA, Sriram K, Meguid MM, Crook M. Refeeding syndrome: treatment considerations based on collective analysis of literature case reports. Nutrition 2010;26(2):156-67. ArticlePubMed
- 6. Camp MA, Allon M. Severe hypophosphatemia in hospitalized patients. Miner Electrolyte Metab 1990;16(6):365-8. PubMed
- 7. Marik PE, Bedigian MK. Refeeding hypophosphatemia in critically ill patients in an intensive care unit. A prospective study. Arch Surg 1996;131(10):1043-7. ArticlePubMed
- 8. Rio A, Whelan K, Goff L, Reidlinger DP, Smeeton N. Occurrence of refeeding syndrome in adults started on artificial nutrition support: prospective cohort study. BMJ Open 2013;3(1):e002173.ArticlePubMedPMC
- 9. Hoffmann M, Zemlin AE, Meyer WP, Erasmus RT. Hypophosphataemia at a large academic hospital in South Africa. J Clin Pathol 2008;61(10):1104-7. ArticlePubMed
- 10. Ormerod C, Farrer K, Harper L, Lal S. Refeeding syndrome: a clinical review. Br J Hosp Med (Lond) 2010;71(12):686-90. ArticlePubMed
- 11. Thompson JS, Hodges RE. Preventing hypophosphatemia during total parenteral nutrition. JPEN J Parenter Enteral Nutr 1984;8(2):137-9. ArticlePubMed
- 12. Miller SJ. Death resulting from overzealous total parenteral nutrition: the refeeding syndrome revisited. Nutr Clin Pract 2008;23(2):166-71. ArticlePubMedPDF
- 13. Hayek ME, Eisenberg PG. Severe hypophosphatemia following the institution of enteral feedings. Arch Surg 1989;124(11):1325-8. ArticlePubMed
- 14. Ebel H, Günther T. Magnesium metabolism: a review. J Clin Chem Clin Biochem 1980;18(5):257-70. ArticlePubMed
- 15. Pham PC, Pham PA, Pham SV, Pham PT, Pham PM, Pham PT. Hypomagnesemia: a clinical perspective. Int J Nephrol Renovasc Dis 2014;7:219-30. ArticlePubMedPMC
- 16. Martin PR, Singleton CK, Hiller-Sturmhöfel S. The role of thiamine deficiency in alcoholic brain disease. Alcohol Res Health 2003;27(2):134-42. PubMedPMC
- 17. Ahn J, Kim JW. Wernicke's encephalopathy in a patient with acute alcoholic pancreatitis. Korean J Med 2008;75(6):700-3.
- 18. Sechi G, Serra A. Wernicke's encephalopathy: new clinical settings and recent advances in diagnosis and management. Lancet Neurol 2007;6(5):442-55. ArticlePubMed
- 19. Veverbrants E, Arky RA. Effects of fasting and refeeding. I. Studies on sodium, potassium and water excretion on a constant electrolyte and fluid intake. J Clin Endocrinol Metab 1969;29(1):55-62. ArticlePubMed
- 20. Klein CJ, Stanek GS, Wiles CE 3rd. Overfeeding macronutrients to critically ill adults: metabolic complications. J Am Diet Assoc 1998;98(7):795-806. PubMed
- 21. National Institute for Clinical Excellence. Nutrition support for adults. Clinical Guideline No. 32. 2006. London: National Collaborating Centre for Acute Care (UK); p. 1-176.
- 22. Assadi F. Hypophosphatemia: an evidence-based problem-solving approach to clinical cases. Iran J Kidney Dis 2010;4(3):195-201. PubMed
- 23. Hur H. Nutrition Screening and Assessment of Patients for Malnutrition;J Korean Soc Parenter Enter Nutr 2013;5(1):2-9.
- 24. Crook MA. Refeeding syndrome: problems with definition and management. Nutrition 2014;30(11-12):1448-55. ArticlePubMed




 E-submission
E-submission KSPEN
KSPEN KSSMN
KSSMN ASSMN
ASSMN JSSMN
JSSMN Cite
Cite